打一针管七天 张力团队为化疗患者带来止吐新选择!
化疗是癌症治疗的常规手段之一,但消灭癌细胞的同时也给患者带来了极大的痛苦,其中,恶心呕吐是化疗期间最明显的副反应之一,部分患者甚至因为恶心呕吐带来的不适,而放弃化疗。
2024年12月2日,中山大学肿瘤防治中心张力教授团队牵头开展、全国67家研究中心共同参与的“评价注射用HR20013用于预防高致吐性化疗引起恶心呕吐的有效性和安全性研究——多中心、随机、双盲双模拟、阳性对照Ⅲ期临床研究(PROFIT)”在国际顶级肿瘤学期刊《临床肿瘤学杂志》(Journal of Clinical Oncology,简称JCO)在线发表。研究结果显示,HR20013预防以顺铂为基础的高致吐化疗导致的恶心呕吐(HEC-CINV)显示出具有前景的临床疗效及可控的安全性,有望为此类患者提供治疗新选择。

中山大学肿瘤防治中心张力教授、黄岩主任医师为该论文的共同通讯作者。周华强主治医师、赵媛媛主任医师为该论文共同第一作者。
化疗相关性恶心呕吐(CINV)是化疗过程中最常见的不良反应之一,不仅使患者对化疗产生恐惧,还会降低治疗依从性,从而影响生存获益。研究表明,以顺铂为代表的高致吐性化疗可使急性呕吐的发生率超过90%,延迟性恶心呕吐的发生率超过50%。目前,国内外指南针对高度致吐性化疗(HEC)相关CINV的预防,推荐以5-羟色胺3受体拮抗剂(5-HT3 RA)和神经激肽受体1拮抗剂(NK-1RA)为基础的三联/四联方案。然而,临床上使用的止吐药大多是半衰期较短的药物,需要长期、反复给药,且多药联合使用较为复杂,导致患者依从性下降,用药方案难以执行。
因此,如何简化临床用药,提高患者的用药依从性,并一次性全面控制肿瘤患者急性期(化疗后0-24h)、延迟期(化疗后24-120h)甚至是超延迟期(化疗后120-168h)的CINV,仍然是亟待解决的临床问题。
新型复方止吐药HR20013由Fosrolapitant和帕洛诺司琼组成,Fosrolapitant在体内可转换为罗拉匹坦。罗拉匹坦和帕洛诺司琼的半衰期分别长达约180小时和40小时。HR20013结合了NK-1RA罗拉匹坦和二代5-HT3RA帕洛诺司琼的超长半衰期优势。前期临床试验表明,HR20013能够同时覆盖急性期、延迟期以及超延迟期,在每个化疗周期仅需用药一次,即可覆盖长达7天的CINV风险期,极大简化了用药方案,同时兼顾了安全性、有效性和患者依从性。然而,该药物在预防HEC相关CINV的有效性和安全性仍需通过更高循证医学证据进行进一步验证。
PROFIT研究是一项多中心、随机、双盲、双模拟、阳性对照的III期临床研究(NCT05509634),共入组754例未经化疗的恶性实体瘤患者,其中750例接受药物治疗。患者随机分为两组,在每周期给与顺铂为基础的高度致吐性化疗(顺铂剂量≥60mg/m2,IV,D1,Q3W,共2个周期)前,分别接受研究药物HR20013或福沙匹坦+帕洛诺司琼(FAPR+PALO)治疗,同时口服地塞米松(DEX;D1-D4),连续观察两个化疗周期。主要终点是第1个化疗周期总体期(0-120h)完全缓解(CR)率。关键次要终点为第1个化疗周期超延迟期完全缓解率。此外,该研究还评估了患者的生活质量,以对日常生活无影响(NIDL)的患者比例作为评估依据。在基线以及开始使用高度致吐性化疗的24h、120h和168h后分别填写呕吐生活功能量表(FLIE)问卷。NIDL定义为总体FLIE评分>108或恶心/呕吐评分>54。
两组患者基线特征具有可比性。HR20013+DEX组和FAPR+PALO+DEX组分别有373例和377例患者接受第1个周期的研究治疗,314例和336例患者接受第2个周期的研究治疗。
第一周期总体期的完全缓解率分别为77.7% vs 78.2%(差异为-0.9%[95% CI:-6.7,5.0];单侧P<0.01),显示主要终点达到非劣效性(图1)。同时,该Ⅲ期临床研究数据显示出了HR20013在超延迟期的疗效,无论是第一周期还是第二周期,HR20013超延迟期完全缓解率数值均高于FAPR+PALO(第一周期:90.3% vs 86.5%;第二周期:92.7% vs 87.8%;图1、2)。
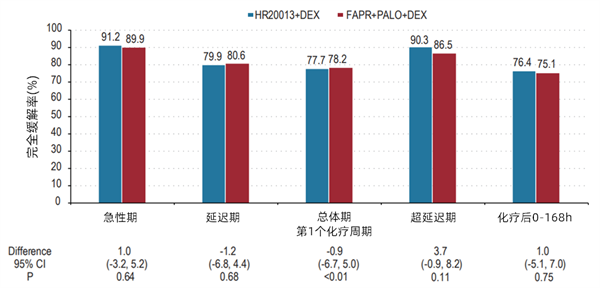
图1 第一周期完全缓解率
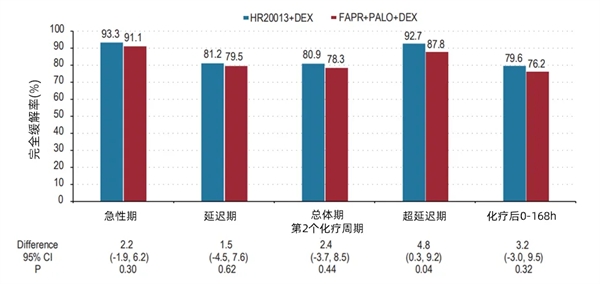
图2 第二周期完全缓解率
在超延迟期阶段,HR20013+DEX组的完全保护率(CP;无呕吐/无挽救治疗/无显著恶心[视觉模拟量表得分<25mm])和完全控制率(TC;无呕吐/无挽救治疗/无恶心[视觉模拟量表得分<5mm])数值上优于对照组,尤其是在第二周期(CP:90.8% vs 86.3%;TC:83.8% vs 78.6%;图3)。
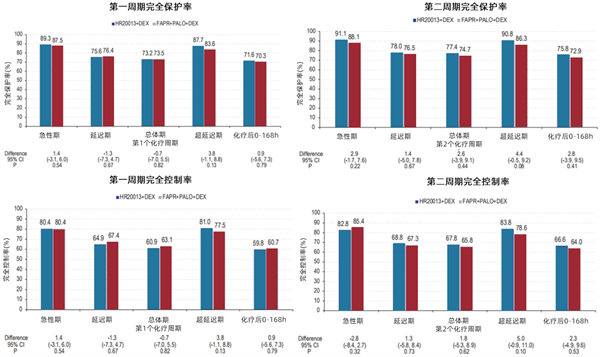
图3 第一周期和第二周期完全保护与完全控制率
在第一周期的3个阶段[急性期、延迟期和超延迟期]中,两组的对日常生活无影响(NIDL)患者比例在整体域、恶心域和呕吐域大体相当(所有的名义双侧P>0.05;图4)。在第二周期中,与FAPR+PALO+DEX组相比,HR20013+DEX组的整体域延迟期(93.6% vs 87.8%;名义双侧P=0.01)、呕吐域延迟期(95.2% vs 90.8%;名义双侧P=0.03)、整体域超延迟期(96.8% vs 92.9%;名义双侧P=0.03)、恶心域超延迟期(95.9% vs 91.1%;名义双侧P=0.02)对日常生活无影响(NIDL)患者比例更高(图5)。

图4 第一周期基于FLIE评分的对日常生活无影响患者比例
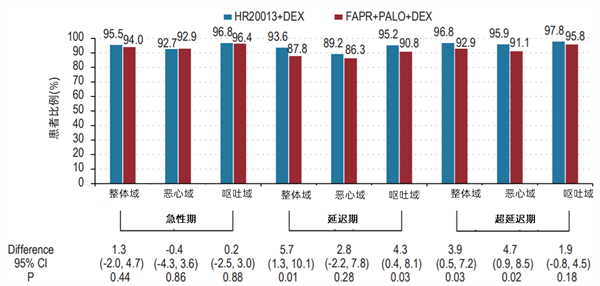
图5 第二周期基于FLIE评分的对日常生活无影响患者比例
HR20013+DEX组治疗相关不良事件(TRAEs)的发生率在第一周期为35.7%,在整个研究期间为42.1%,而FAPR+PALO+DEX组分别为38.2%和44.0%。在整个研究期间,最常见的不良反应是便秘(HR20013+DEX:10.7%,FAPR+PALO+DEX:14.3%)和呃逆(HR20013+ DEX:7.5%,FAPR+PALO+DEX:11.4%)。
综上,HR20013+DEX在预防恶心呕吐的疗效不劣于FAPR+PALO+DEX,并且具有良好的安全性。此外,研究还发现HR20013+DEX可能在超延迟期提高临床获益。与FAPR+PALO+DEX相比,HR20013+DEX在接受HEC化疗的患者中显示出改善生活质量的潜力,尤其是在延迟期和超延迟期。
基于HR20013在预防高致吐化疗导致的恶心呕吐(HEC-CINV)取得的良好成果,目前该创新药物的首批适应症上市申请已被国家药品审评中心(CDE)受理。我们期待该药物尽快获得适应症批准,造福广大患者!
研究者简介:

通讯作者 张力
中山大学肿瘤防治中心内科主任导师、博士生导师、二级教授、肺癌首席专家,中国抗癌协会(CACA)肿瘤药物临床研究专业委员会候任主任委员,中国临床肿瘤学会(CSCO)免疫治疗专家委员会候任主任委员,中国临床肿瘤学会非小细胞肺癌专家委员会副主任委员,中国临床肿瘤学会肿瘤支持与康复治疗专家委员会副主任委员,广东省医学会临床研究学分会主任委员,广东省临床医学会精准医学分会主任委员。

共同通讯作者 黄岩
中山大学肿瘤防治中心内科主任医师,中国抗癌协会癌症康复与姑息治疗专业委员会副主任委员,中国抗癌协会肿瘤药物临床研究专业委员会委员,中国临床肿瘤学会肿瘤支持与康复治疗专家委员会常务委员,广东省抗癌协会化疗专业委员会常务委员,广东省抗癌协会癌症康复与姑息治疗专业委员会常务委员。

共同第一作者 周华强
中山大学肿瘤防治中心内科肿瘤学博士、主治医师、科秘书,中山大学肿瘤防治中心优秀青年提升计划入选者,中国临床肿瘤学会“全国35位最具潜力青年肿瘤医生”,中国南方肿瘤临床研究协会肺癌专业委员会委员。

共同第一作者 赵媛媛
中山大学肿瘤防治中心内科博士,主任医师,硕士生导师。中国抗癌协会安宁疗护专业委员会委员,广东省抗癌协会癌症康复与姑息治疗专业委员会委员,广东省抗癌协会癌症康复与姑息治疗专业委员会青年委员会常委,广东省抗癌协会化疗专业委员会青年委员会常委
论文链接:
https://ascopubs.org/doi/10.1200/JCO-24-01308
(责任编辑:家医在线 通讯员:文朝阳、陈鋆、赵现廷)
专家答疑
抑郁症能治好吗?怎么治
2024-12-12榆林哪家硬起困难医院看的好
2024-12-12精神科医生在线咨询
2024-12-12榆林那里看早泄最好
2024-12-12焦虑症怎么治疗最好的方法
2024-12-12济南神安医院是正规医院吗
2024-12-12精神分裂的原因
2024-12-12得白癜风能吃零食吗
2024-12-11


